Die Rolle der Epigenetik in Gefässerkrankungen
Epigenetische Prozesse spielen eine entscheidende Rolle in der Regulierung der Genexpression auf der Chromatinebene und deren Deregulierung trägt massgeblich zu unterschiedlichen Erkrankungen oder zu deren Verschlimmerung bei.
Durch verschiedene Modifizierungen des Chromatins, insbesondere der Histone, und der DNA (Methylierung, Acetylierung, Physphorylierung, Ubiquitinierung) verändert sich die Struktur des Chromatins (kompakt, offen) und dadurch die Zugänglichkeit von Transkriptionsfaktoren zu den einzelnen Genen, vorzugsweise deren Promotorenregion. Dadurch kann die Genexpression entscheidend geprägt werden. Chronische Erkrankungen, atherosklerosische Veränderungen in der Gefässwand, überschüssige Entzündungsreaktionen und andere Faktoren können epigenetische Regulation in Mitleidenschaft ziehen, was häufig den Verlust des Gleichgewichts in der Expression vieler Gene zur Folge hat.
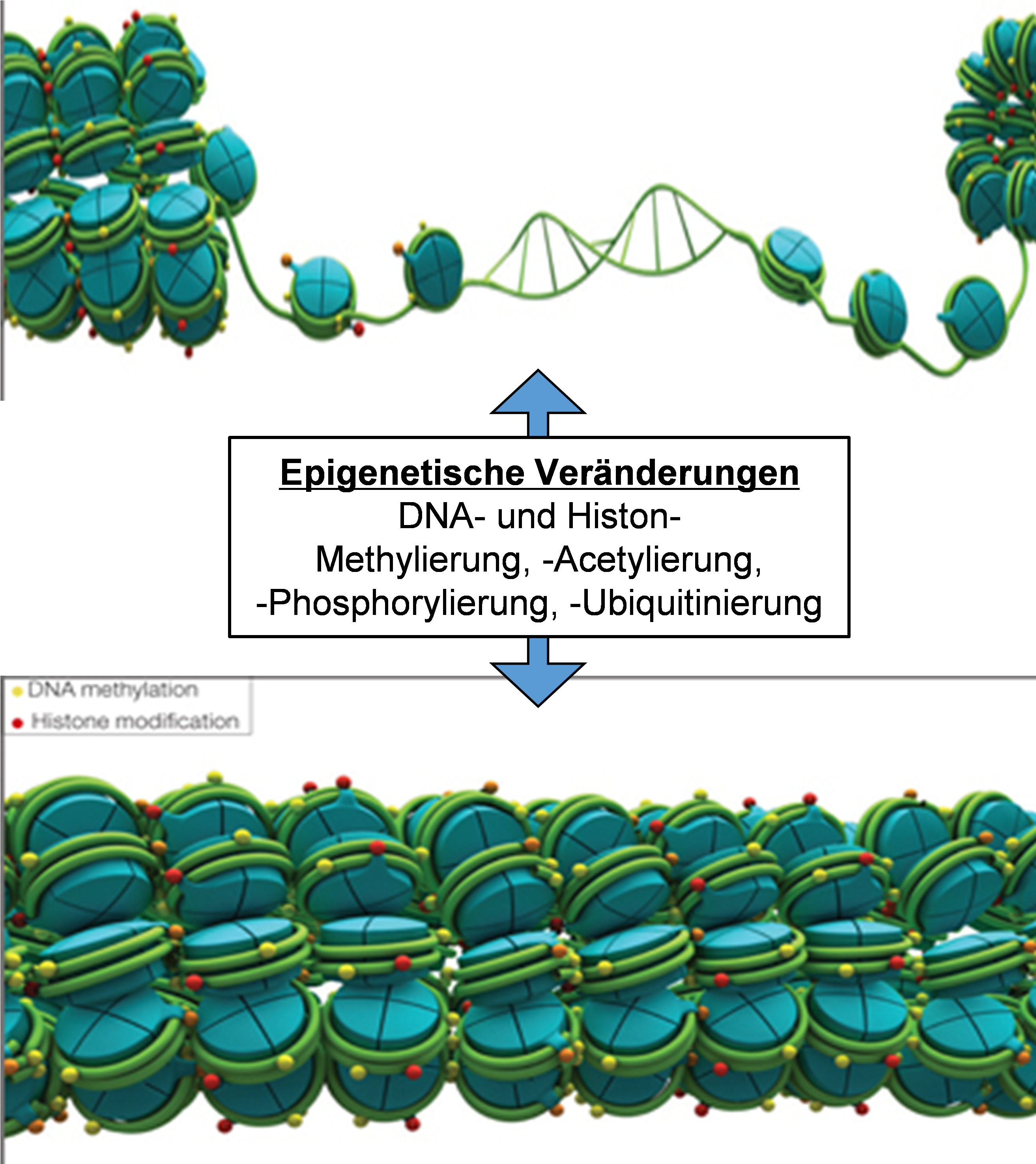
Im Falle von Atherosklerose oder Aneurysma führen diese krankhafte Veränderungen des Epigenoms unter anderem zur Überexpression verschiedener proteolytischer Enzyme, verstärkter Degradierung der extrazellulären Matrix (Kollagen, Elastin, Proteoglykane) und folglich zur Schwächung der Gefässwand. Diese Umstände beschleunigen die Progression der Atherosklerose und die Erweiterung der Aorta, bis schliesslich, z.B. durch eine Ruptur, ein schwerwiegendes klinisches Ereignis entsteht.
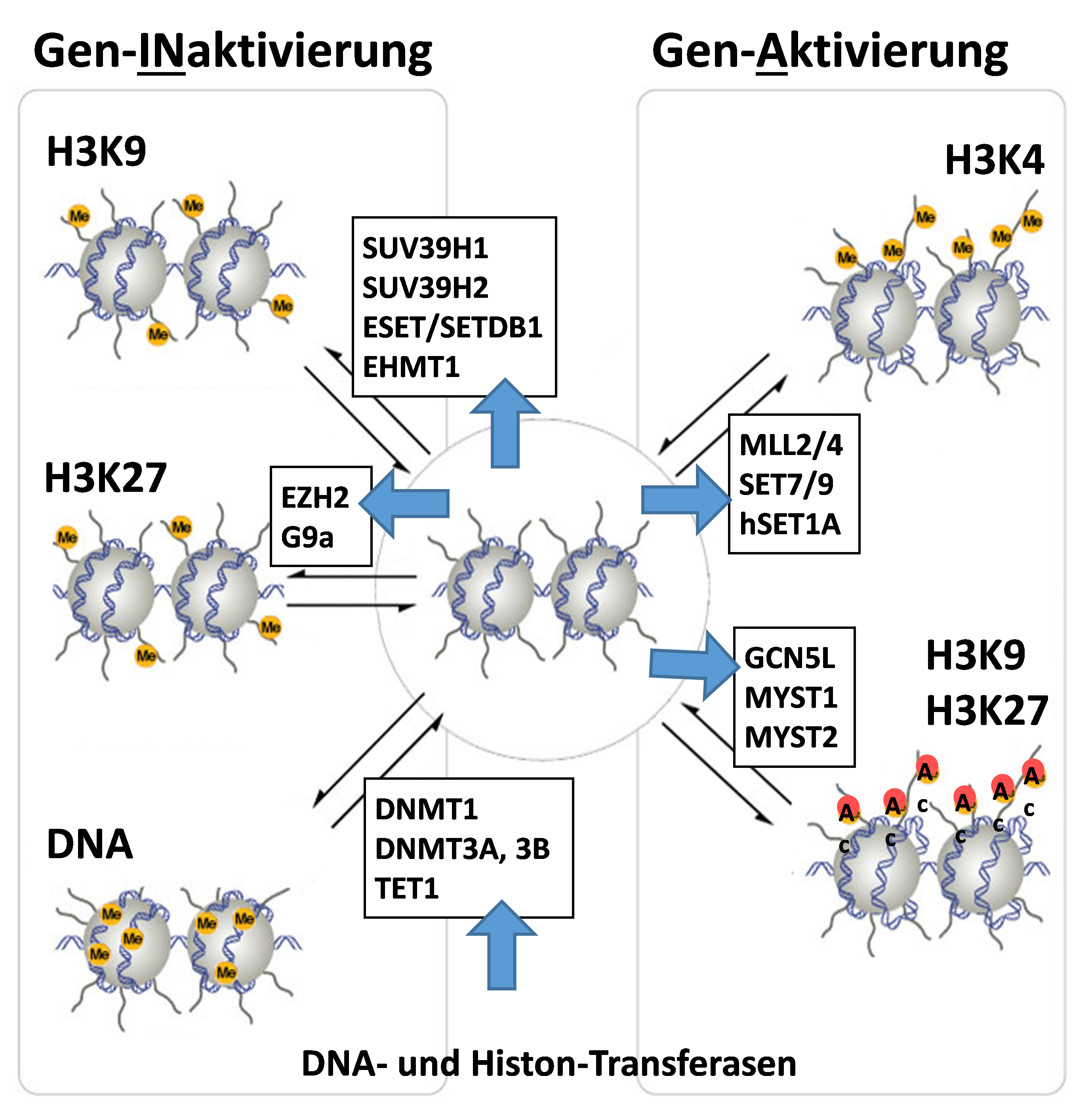
Unsere Ergebnisse haben deutlich gezeigt, dass sich sowohl die DNA-Methylierung, als auch Histon-Methylierung und -Acetylierung signifikant mit dem Fortschreiten von Atherosklerose verändern [Xu 2019, Xu 2018, Greißel 2016, Culmes 2015, Pelisek 2012]. Diese Veränderungen waren nicht nur im Gewebe von Patienten mit hochgradiger Carotisstenose, sondern auch im Blut der betroffenen Individuen zu verzeichnen. Das Gleiche gilt auch für fortgeschrittene AAAs, wo wir nicht nur signifikante Veränderungen in Histon-Methylierung und -Acetylierung beobachtet haben, sondern auch in der Expression korrespondierender Methyl- und Acetyl-Transferasen [Xu 2018, Han 2016].
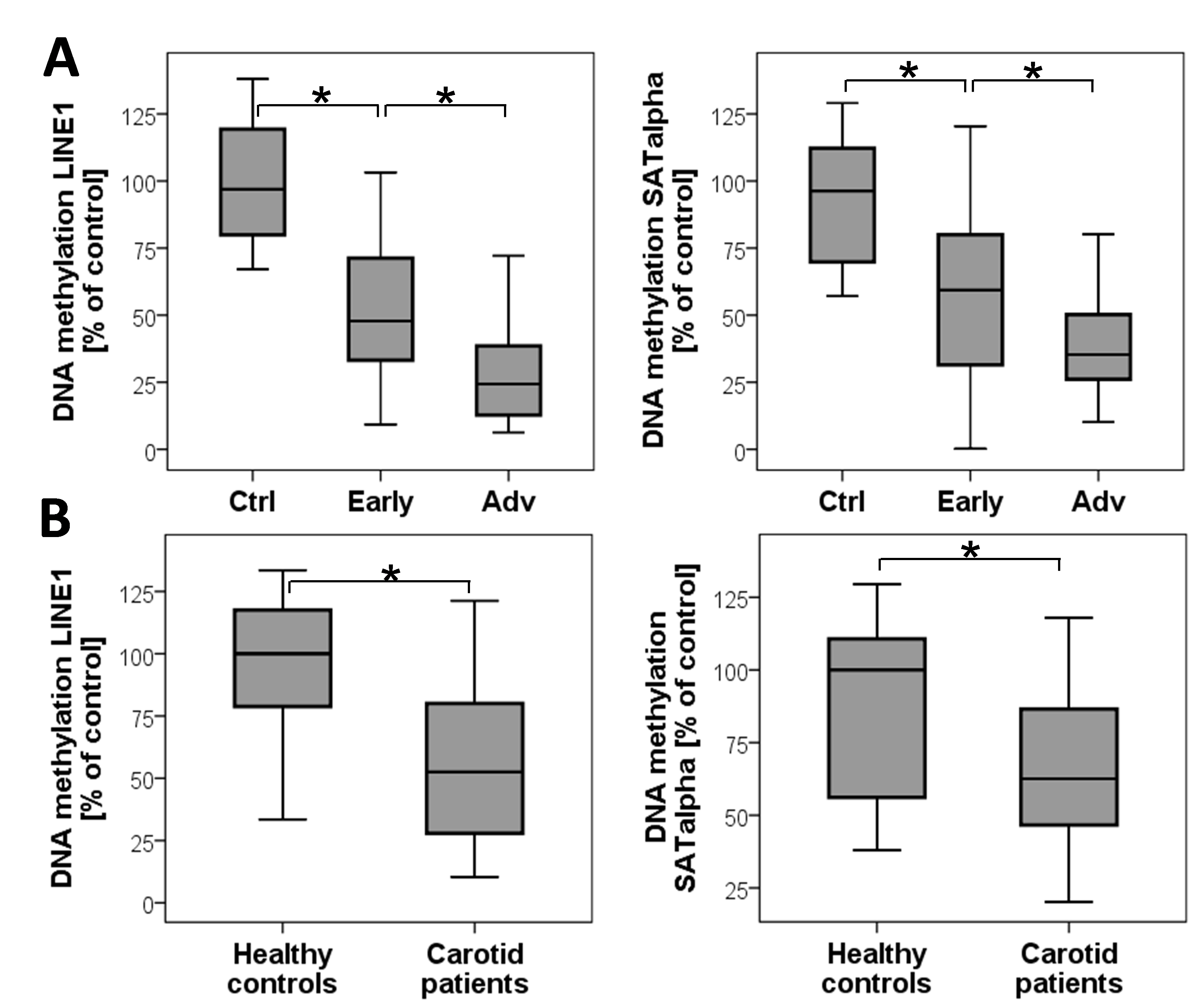
DNA-Methylierung in Carotisplaques (A) und im Blut (B) korresondierender Patienten mit hochgradiger Carotisstenose. Quantifizierung wurde auf ALU1 normaliziert. Das Ausmass der DNA-Methylierung wurde auf die Methylierung der DNA gesunder Gefässe bezogen und als 100% gesetzt (Greißel 2016).

Zelluläre Lokalisierung von Histon-Acetyltransferase KAT3B in AAA (Übersichtsbild: Hämalaun-Eosin, Massstab 1000 µm) (Han 2016).
- Xu S, Kamato D, Little PJ, Nakagawa S, Pelisek J, Jin ZG. Targeting epigenetics and non-coding RNAs in atherosclerosis: from mechanisms to therapeutics. Pharmacol Ther. 2019;196:15-43.
- Xu S, Pelisek J, Jin ZG. Atherosclerosis is an epigenetic disease. Trends Endocrinol Metab. 2018;S1043-2760(18)30090-0.
- Xu S, Xu Y, Yin M, Zhang S, Liu P, Koroleva M, Si S, Little PJ, Pelisek J, Jin ZG. Flow-dependent epigenetic regulation of IGFBP5 by H3K27me3 contributes to endothelial anti-inflammatory effects. Theranostics. 2018;8(11):3007-3021.
- Greißel A, Culmes M, Rudelius M, Burgkart R, Zernecke A, Eckstein HH, Pelisek J. (2015) Histone acetylation and methylation in high graded carotid plaques. Cardiovasc Pathol, 2016;25(2):79-86.
- Han Y, Tanios F, Reeps C, Zhang J, Schwamborn K, Lutz B, Eckstein HH, Zernecke A, Pelisek J. Histone acetylation and expression of corresponding histone acetyl-transferases in human abdominal aortic aneurysm. Clin Epigenetics. 2016; 8:3.
- Culmes M, Greißel A, Napieralski R, Dushenalieva S, Wagner E, Gebhard H, Schmidt M, Eckstein HH, Zernecke A, Pelisek J. DNA methylation in carotid plaques is associated with severity of atherosclerosis and reduced expression of DNA methyltransferases. Thromb Haemost. 2015;21:114(2).
- Yan X, Ehnert S, Culmes M, Claudine C, Schyschka L, Wang Z, Stöckle U, De Sousa PA, Pelisek J, Nussler AK. Small molecule epigenetic inhibitors improve osteogenic differentiation of aged human adipose-derived mesenchymal stem cells by DNA demethylation. PLoS One. 2014;9(6):e90846.
- Culmes M, Eckstein HH, Burgkart R, Nüssler AK, Guenther M, Wagner E, Pelisek J. Endothelial differentiation of Adipose derived mesenchymal stem cells is improved by BIX-01294, an epigenetic modifying drug. Eur J Cell Biol. 2013;92(2):70-79.
- Pelisek J, Eckstein HH, Zernecke A. (2012) Pathophysiological mechanisms of carotid plaque vulnerability: impact on ischemic stroke. Arch Immunol Ther Exp. 2012;60(6):431-442.